Um dos maiores desafios no tratamento do câncer é que a mesma terapia pode ser altamente eficaz para alguns pacientes, enquanto falha completamente para outros. Um novo estudo publicado na Nature Communications, liderado pela Dra. Louise Fets no Laboratório de Ciências Médicas do MRC (LMS), analisa mais de perto por que isso acontece. Os pesquisadores se concentraram nos inibidores de PARP, uma classe de medicamentos direcionados ao câncer, e acompanharam como eles se movem através de amostras de tumor ovariano utilizando ferramentas de imagem avançadas.
Os resultados mostram que esses medicamentos podem se acumular dentro de lisossomos, pequenas estruturas nas células que atuam como “centros de reciclagem”. Uma vez dentro, os medicamentos podem ficar presos e depois serem liberados, influenciando a eficácia do tratamento.
Mapeando Como os Medicamentos contra o Câncer se Espalham Dentro dos Tumores
As opções de tratamento para câncer se expandiram rapidamente nos últimos anos, melhorando os resultados para muitos pacientes. Os inibidores de PARP, em particular, transformaram o tratamento para câncer de ovário. No entanto, nem todos os pacientes se beneficiam, e alguns desenvolvem resistência ao longo do tempo. Para que esses medicamentos funcionem, eles devem se acumular dentro das células cancerígenas em níveis suficientemente altos para desencadear a morte celular. Apesar disso, os cientistas ainda têm um entendimento limitado de como os medicamentos se distribuem dentro dos tumores e o que controla esse processo.
Esta pesquisa mostra que a eficácia depende não apenas de se um medicamento alcança um tumor, mas também de como ele se espalha dentro dele e dentro de células individuais. Para estudar isso, os pesquisadores utilizaram finas fatias de tumores ovarianos retirados de pacientes e mantidos vivos no laboratório. Essas amostras, conhecidas como “explantes”, foram tratadas com inibidores de PARP para que os cientistas pudessem observar diretamente como os medicamentos se moviam através do tecido tumoral humano real.
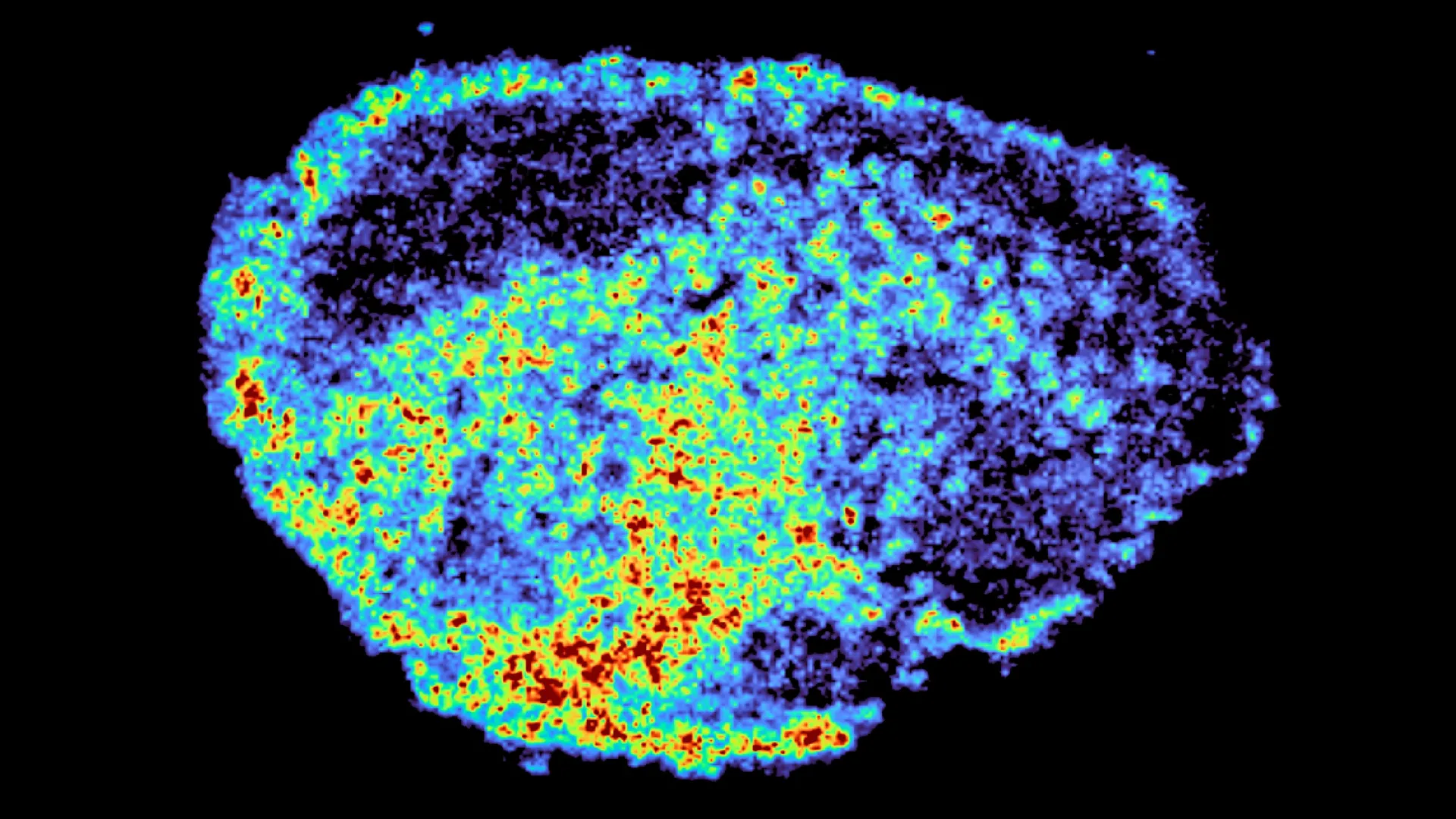
Usando imagens por espectrometria de massas, a equipe produziu mapas detalhados mostrando exatamente onde os medicamentos se acumulavam. Eles combinaram isso com transcriptômica espacial, o que permitiu examinar a atividade genética em áreas com altos e baixos níveis de medicamentos dentro da mesma amostra. Os resultados revelaram diferenças significativas na distribuição do medicamento, tanto dentro de tumores individuais quanto entre os pacientes, mesmo quando a mesma dose foi utilizada.
“Um aspecto inovador deste estudo foi o uso da imagem por espectrometria de massas para medir e visualizar diretamente a absorção do medicamento no tecido tumoral do paciente. Através do mapeamento espacial das moléculas do medicamento, pudemos identificar regiões de alta e baixa concentração do mesmo e comparar a expressão gênica, a partir da mesma fatia de tecido, usando transcriptômica espacial”, diz a Dra. Zoe Hall, autora sênior e Professora Associada no Departamento de Metabolismo, Digestão e Reprodução do Imperial.
Lisossomos Agem como Reservatórios Ocultos de Medicamentos
Os pesquisadores descobriram que os lisossomos desempenham um papel central nessa distribuição desigual. Alguns inibidores de PARP são atraídos para esses compartimentos e armazenados lá em vez de se espalharem uniformemente por toda a célula. Isso cria bolsões internos onde os medicamentos se acumulam.
Esses lisossomos atuam como reservatórios de liberação lenta – retendo o medicamento e liberando-o gradualmente – o que aumenta a exposição em certas células, enquanto deixa outras com níveis muito mais baixos. Nem todos os inibidores de PARP se comportam da mesma maneira. O estudo encontrou que medicamentos como rucaparib e niraparib são afetados por esse processo, enquanto outros como olaparib não são.
“Ficamos surpresos ao ver uma grande variabilidade na acumulação do medicamento em nível de única célula. Essa variabilidade foi impulsionada pelo acúmulo do medicamento nos lisossomos, que estão atuando como reservatórios, aumentando a exposição das células cancerígenas aos medicamentos, armazenando e liberando o medicamento quando necessário”, diz a Dra. Carmen Ramirez Moncayo, primeira autora e Pesquisadora Pós-Doutoral no LMS.
O que isso Significa para o Futuro do Tratamento do Câncer
Os inibidores de PARP já são amplamente utilizados para tratar cânceres de ovário, mama e próstata, e estão sendo testados em muitos outros tipos de câncer. Compreender melhor como esses medicamentos são armazenados e distribuídos dentro das células pode levar a estratégias de tratamento mais personalizadas, melhorando a eficácia enquanto reduz a resistência e a recaída.
“Ao entender como os medicamentos são absorvidos pelas células, podemos entender se isso influencia o motivo pelo qual os medicamentos contra o câncer funcionam para algumas pessoas e não para outras. Eventualmente, esperamos poder estudar a assinatura molecular do tumor de um paciente para ajudar a personalizar as abordagens terapêuticas de uma maneira mais individualizada”, diz a Dra. Louise Fets, autora sênior e Chefe do Grupo de Transporte de Medicamentos e Metabolismo Tumoral do LMS.
Este estudo foi realizado utilizando tecido tumoral mantido fora do corpo. Em pacientes reais, os medicamentos são administrados através da corrente sanguínea, e os vasos sanguíneos tumorais muitas vezes são desorganizados, o que pode contribuir ainda mais para a distribuição desigual do medicamento. Estudos futuros utilizarão modelos animais e grupos maiores de pacientes para entender melhor como a entrega do medicamento, a estrutura do tumor e o armazenamento lisossomal interagem em cenários clínicos, incluindo em cânceres recorrentes.
Esta pesquisa foi apoiada por financiamento do Conselho de Pesquisa Médica, Pesquisa do Câncer no Reino Unido, uma bolsa de doutorado da Parceria de Treinamento em Toxicologia Integrativa administrada pela Unidade de Toxicologia do MRC, e um Prêmio de Desenvolvimento de Carreira do Fundo Global da Victoria’s Secret para Cânceres Femininos, em parceria com Pelotonia e AACR.